UNIST(총장 정무영) 생명과학부의 이창욱 교수팀은 GIST(총장 김기선) 생명과학부의 전영수 교수팀과 공동으로, ‘자가포식이 단백질의 4차 구조(protein quaternary structure)를 통해 조절된다’는 사실을 규명했다. 어떤 물질을 분해할지 선택하고 리소좀으로 옮기는 데 단백질 복합체의 구조가 큰 역할을 하고 있었던 것이다. 향후 자가포식 관련 질환 연구에 새로운 방향을 제시할 것으로 기대된다.
자가포식은 세포가 항상 일정한 상태를 유지해 생존하기 위한 작용이다. 이 작용에 문제가 생기면 파킨슨병이나 치매 같은 퇴행성 신경질환, 염증성 소화기질환, 암, 노화 등이 발생할 수 있다.
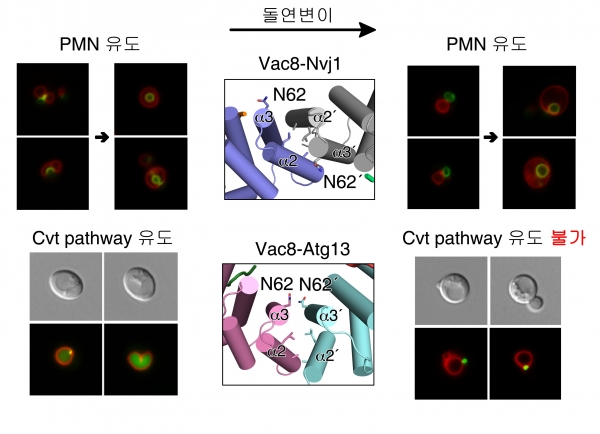
세포 내 불필요한 물질을 골라내 리소좀까지 옮기는 데는 다양한 단백질이 관여한다. 대표적으로 ‘Vac8(Vacuole related 8) 단백질’이 잘 알려져 있는데, 이 단백질이 어떤 단백질과 결합하느냐에 따라 자가포식 유형이 결정된다. 가령 Vac8 단백질이 Nvj1(Nucleus-vacuole junction 1) 단백질과 결합하면 세포핵 일부분을 분해하는 자가포식(PMN)이 작동하는 반면, Atg13(Autophagy Related 13) 단백질과 결합하면 세포질 가수분해 효소를 리소좀으로 수송하는 ‘Cvt 경로(Cytoplasm-to-vacuole targeting pathway)’를 작동시킨다. 하지만 Vac8가 단백질이 이들 단백질과 결합하는 구체적인 원리는 밝혀지지 않았다.
이번 연구에서는 단백질 결정을 이용한 ‘X-선 결정법’과 ‘X-선 소각 산란 분석법’을 이용해 Vac8 단백질이 결합하는 단백질에 따라 4차 구조가 달라진다는 사실을 밝혀냈다. 달라진 구조에 따라 자가포식의 유형도 결정됐다.
 번역 제공
번역 제공

