암의 크기가 커지는 것(증식)과 암이 다른 조직으로 확장되는 것(전이)은 엄연히 다르다. 하지만 이 둘은 간혹 동일한 것으로 치부되기도 한다. 암의 크기가 커진 건 암이 다른 조직으로도 옮겨 갔기 때문이 아니냐고 말이다. 물론 그런 경우도 있다. 대개 암이 우리 몸에 발생했을 경우, 암의 크기가 커질수록 주변의 림프절(조직과 조직을 연결하는 림프관의 곳곳에 있는 둥근 조직)과 다른 조직으로 전이될 확률도 함께 높아진다. 그래서 ‘암의 크기가 커졌다=암이 다른 조직으로 전이됐다’가 통념으로 자리 잡았다.
하지만 이런 통념 때문에 암의 크기가 작은 것을 보고 안심했다가, 다른 조직으로 암이 전이돼 심각한 상황에 처하게 되는 암환자들이 더러 있다. 이런 상황은 암의 크기가 커지지 않고 여전히 작은 크기임에도 불구하고, 주변의 림프절과 다른 조직으로 전이되는 경우가 존재한다는 것을 증명한다. 이는 암 전이와 암 증식 사이에 우리가 여전히 알지 못하는 ‘비밀’이 숨겨 있는 것은 아닐까라는 궁금증을 불러일으킨다.

이 궁금증을 해결해줄 한 편의 논문이 지난달 12일 <네이쳐 커뮤니케이션즈>에 실렸다. 이 논문을 작성한 육종인 연세대 교수(치과대학) 연구팀은 암세포 ‘증식’을 조절하는 ‘히포(Hippo)’ 신호전달과 암세포 ‘전이’에 관여하는 ‘윈트(Wnt)’ 신호전달의 상호조절 관계를 규명했다. ‘전이’에 관여하는 윈트 신호전달의 활성인자인 디셰벌드(Dishevelled)가 ‘증식’을 조절하는 히포 신호전달의 조절인자인 YAP의 활성을 조절한다는 것을 밝혀낸 것이다.
연구 결과에 따르면, 디셰벌드는 ‘인산화’된 형태의 YAP과 결합할 경우, 세포핵 밖으로 이동하게 돼 암세포의 증식을 조절하는 YAP이 활성화되지 못하도록 막는다. 여기서 인산화는 인의 산소산인 인산이 물질에 붙는 것을 말하며, 많은 단백질이 이 인산화를 통해 자신의 생물활성을 조절한다. YAP은 암을 유발하는 단백질의 일종이기도 하다.
하지만 디셰벌드가 YAP을 억제하지 않으면, 암세포 전이에 관여하는 윈트 신호와 암 증식을 조절하는 YAP이 동시에 활성화가 돼, 확연하게 암의 크기가 커지게 된다. 즉 YAP을 인산화 시키느냐가 암의 크기를 조절하는 데 관건인 것이다. 그런데 이 YAP의 인산화에 관여하는 것이 바로 종양억제인자(p53 또는 LKB1)다. 이 종양억제인자가 손실됐을 경우, YAP은 인산화 되지 못하고, 인산화되지 못한 YAP은 디셰벌드와 결합하지 못하게 돼 암의 크기가 커지게 된다.
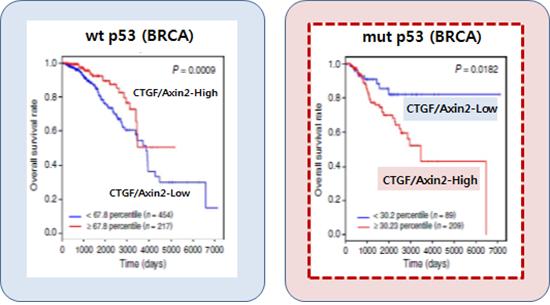
육종인 교수는 “이번 연구는 암세포의 전이와 증식을 유기적으로 조절하는 신호전달 조절 과정을 규명한 것으로, 암을 치료한 뒤의 경과를 예측하는 데 필요한 지표를 제공할 수 있을 것으로 기대된다”며 연구 의의를 밝혔다. 종양억제인자, YAP의 인산화, 디셰벌드와 인산화된 YAP의 결합 등이 암 완치의 한 지표로서 활용될 수 있을 것이다. 다음은 육종인 교수와의 일문일답.
Q. 암은 대체 무엇인가?
암은 조절되지 않는 증식이다. 만약 손가락을 베었다고 하자. 시간이 지나면 그 주변의 조직들이 증식해 상처 난 손가락을 아물게 한다. 이 증식이라는 과정은 모든 생명체의 정상적인 특성이다. 하지만 이런 증식도 언제나 조절을 받게 된다. 이 점이 중요하다. 상처 난 손가락 주변의 조직도 상처가 아문 뒤에는 증식하지 않는다. 그런데 암은 조절되지 않고 증식을 계속하는 것이다.
Q. 그때 종양억제인자가 작동해야 하는 것 아닌가.
그렇다. 그때 종양억제인자가 증식을 제어(조절)해야 한다. 그래서 이 종양억제인자를 컨트롤 타워라 부를 수 있고, 모든 세포가 갖고 있는 것이기도 하다. 이번 연구를 진행하며 품고 있던 의문은 ‘왜 종양억제인자가 없어지면, 조절되지 않는 증식, 즉 암이 발생하는가’였다.
Q. 그 의문을 디셰벌드, YAP 등이 관여한 매커니즘으로 상당 부분 해소했다. 향후 어떤 연구를 진행할 생각인가?
20년 넘게 발표한 연구의 대부분이 암이나 신체 신호전달 물질에 대한 것이었다. 그런데 이 연구들이 가능했던 것은 국민의 세금을 연구비로 지원받았기 때문이다. 그래서 보다 많은 분들의 삶에 도움이 될 만한 연구를 해야 하지 않을까라는 생각을 하고 있다. 최근 치료제 개발에 관심을 두는 것도 그 이유 때문이다. 하지만 치료제 개발도 만만치 않다. 막대한 연구비를 투입했음에도 성공하지 못할 가능성이 크기 때문이다. 지금 당장은 치료제 개발에 필요한 기초연구들을 최대한 해놔야겠다는 계획이다.
Q. 하지만 이런 연구결과를 비전공자들이 접했을 경우, 암에 대해 전보다 안심할 것 같다.
겨우 한 발짝 내딛은 것에 불과하다. 이제 산 하나 넘었다고 생각해주시는 게 정확하다.
Q. 사실 ‘치과대학에서도 암 연구를 하나’라는 생각이 들었다.
많은 분들이 놀라는 점이기는 하다. 하지만 과거와 달리 요즘은 유전자 수준에서 병에 접근하기 때문에 치과대학에서든, 수의대학에서든, 생명과학과에서든 병에 대해 연구할 수 있다. 과거에는 컴퓨터공학에서만 인터넷 연구를 했지만, 요즘에는 컴퓨터공학뿐만 아니라 거의 모든 학문에서 인터넷 연구를 하는 것과 비슷하다고 보면 된다. 특히 누구나 NIH(미국 국립보건원)에서 유전자 관련 정보를 얻을 수 있어, 관심만 있다면 유전자 수준에서 병을 연구할 수 있는 시대가 된 것이다.
양도웅 기자 doh0328@kyosu.net
 번역 제공
번역 제공

